
Full Service CRO
Monitorización remota, patient centricity, TMF electrónico, ensayos clínicos descentralizados… El sector de la salud en general y la industria farmacéutica en particular están asistiendo a un auténtico cambio de paradigma. En Sermes CRO vamos de la mano de estos avances, por eso en nuestros 25 años de historia hemos evolucionado, pasando de ser la CRO tradicional de nuestros inicios a una CRO donde la tecnología juega un papel fundamental a la hora de optimizar procesos para nuestros clientes.
Ofrecemos soluciones personalizadas, que van desde el mismo planteamiento inicial del protocolo de un ensayo clínico hasta cubrir por completo el ciclo de desarrollo de medicamentos y terapias. Puedes confiar en que nuestro apoyo científico, clínico y regulatorio, basado en un sólido know-how de la investigación clínica, va a acelerar tus ensayos clínicos y asegurar su calidad y cumplimiento normativo.
More than 1800 clinical trials submitted in the last five years
Actividades

Consultoría Clínica

Unidad de Bioestadística y Gestión de datos

Control de Calidad

Unidad Regulatoria

Farmacovigilancia

Unidad de Contratos & Facturación
Consultoría Clínica
Sermes CRO cuenta con una experiencia de 25 años desarrollando investigación clínica en prácticamente todas las áreas terapéuticas, adaptada a todo tipo de clientes.
Desde nuestra unidad de Consultoría Clínica, nos encargamos de ayudar a nuestros clientes a desarrollar la estrategia de investigación más eficiente en función de los objetivos marcados. De esta forma, conseguimos que nuestros clientes tengan la mejor estrategia posible, que sea competitiva económicamente y en el menor tiempo posible, así como con la máxima calidad que nos exige el mundo de la investigación clínica.
Una de nuestras fortalezas es el conocimiento en el desarrollo integral de la investigación en todas sus fases, y es por ello por lo que, gracias al desarrollo interno de nuestros procesos en todos los puntos y nuestro maduro sistema de calidad podemos reducir tiempos y ofrecer una excelente calidad, lo que resulta fundamental para nuestros clientes a la hora de confiar en nosotros para sus nuevos lanzamientos.
Nuestro equipo de consultores además cuenta con la figura de Project Controller.
El Proyect Controller actuará como nexo entre nuestra unidad de consultoría, uniéndola figura del tradicional Project Manager con la de Controller financiero. Es decir, un project manager con poder de gestión en el presupuesto del estudio, lo que agiliza enormemente la toma de decisiones en el proyecto. Será la persona punto de contacto principal además de acompañar al cliente en todo el desarrollo del estudio, pudiendo facilitar la comunicación directa con el personal implicado en el estudio, evitando sesgos en las instrucciones de nuestros clientes. El Project controller, además se encargará como controller, de asegurar la gestión económica del estudio de la forma más eficiente desde el inicio hasta el final del mismo, así como el control del proyecto en todos sus ámbitos5
- Elaboración de la estrategia de investigación clínica
- Diseño del ensayo clínico
- Control del proyecto
Unidad Regulatoria
¡Te ayudamos a plantear la mejor estrategia regulatoria para acelerar tus ensayos clínicos! Agilizar la aprobación de tus ensayos clínicos es nuestra razón de ser. Somos conscientes de que realizar un ensayo clínico no sólo requiere adoptar el enfoque científico adecuado, sino que es necesario también plantear una estrategia regulatoria ganadora. En Sermes CRO contamos con una amplia y sólida experiencia en asuntos regulatorios, ya que llevamos 24 años ofreciendo servicios de Puesta en Marcha de ensayos clínicos. Convertimos tu objetivo clínico en el nuestro propio. El cumplimiento normativo de tus ensayos clínicos es nuestra mayor fortaleza.
Para ello contamos con un equipo único: flexible, con una gran capacidad de adaptación y totalmente orientado a la resolución de dificultades. Somos un partner de confianza, por eso trabajamos con los laboratorios farmacéuticos más importantes (nuestros clientes están en el top 10), así como con biotecnológicas e investigadores independientes. La clave está en la combinación perfecta de nuestro profundo conocimiento del marco regulatorio (tan cambiante) y nuestras herramientas internas, desarrolladas ad hoc para acelerar los tiempos de tus ensayos clínicos.
Tras analizar pormenorizadamente tus necesidades, establecemos la estrategia de Puesta en Marcha adecuada para tu ensayo clínico. Podemos ayudarte tanto en la presentación y gestión de contratos como en todos estos servicios:
- Servicios CTIS & CTR 536/2014
- Soluciones de reembolso a pacientes: aplicación de desarrollo propio que permite reducir los costes de gestión en investigación clínica
- Solicitud de número EudraCT, preparación de XML
- Gestión de póliza de seguros
- Gestiones con Comités Éticos, EMA, FDA, AEMPS (y demás agencias reguladoras locales), Ministerio de Medio Ambiente…
- Preparación de Financial Reports
- Gestión de contratos con hospitales, investigadores e instituciones colaboradoras
- Soluciones de pagos a hospitales, investigadores… (en cualquier divisa).
- Registro y actualización en bases de datos globales, europeas y en registros nacionales de ensayos clínicos (como ClinicalTrials.gov)
The flexibility, adaptability and problem-solving outlook of our team is our best way to ensure service quality
Unidad de Monitorización
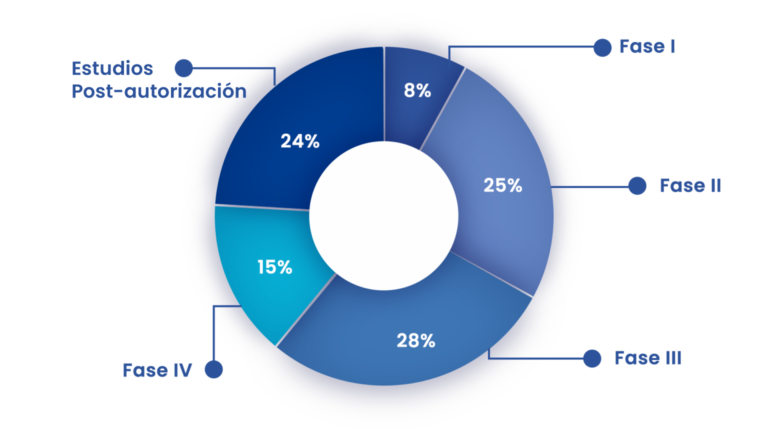
Tenemos claro que aplicar un estricto protocolo de monitorización es la única manera de desarrollar un ensayo clínico. Con Sermes CRO, te aseguras de que se cumplen con todos los requisitos – que no son pocos – a la hora de monitorizar tus ensayos clínicos: seguridad del paciente, cumplimiento del protocolo e integridad de los datos, Buena Práctica Clínica, normativa y todo ello con la calidad que requiere este servicio. Nuestro equipo – altamente cualificado y compuesto por profesionales titulados en ciencias de la salud – tiene amplia experiencia en prácticamente todas las áreas terapéuticas, en ensayos desde fase I a IV y otras investigaciones clínicas como estudios no intervencionales, dispositivos médicos, etc.
Además de trabajar con laboratorios farmacéuticos y compañías biotecnológicas, también nos hemos especializado en colaborar con investigadores independientes, fundaciones, grupos cooperativos e instituciones públicas.
- Viabilidad (feasibility) y selección de centros.
- Planificación de reuniones de investigadores.
- Visitas pre-estudio, de iniciación, monitorización y cierre (visitas presenciales y remotas)
- Gestión de archivos, material del estudio, envíos y medicamentos.
- Gestión de proyectos (tanto para centros como para promotores).
- Preparación y apoyo en auditorías/inspecciones.
Unidad de Bioestadística y Gestión de datos
Somos conscientes de que ser precisos y rigurosos a la hora de gestionar los datos es la única manera de obtener resultados fiables. Nuestra Unidad de Bioestadística y Gestión de Datos – formada por estadísticos, especialistas en biometría, gestores de datos, revisores de datos y docentes universitarios – acumula una extensa experiencia en la gestión de datos de calidad, así como en el análisis de procesos.
Creemos firmemente en aplicar un correcto enfoque estadístico y biométrico ya desde la misma concepción del protocolo, una estrategia ganadora si se trata de obtener conclusiones precisas y consistentes. Lógicamente, la consistencia de los datos y su adecuada gestión es clave durante todo el desarrollo de cualquier ensayo clínico.
Nuestro equipo de bioestadísticos y gestores de datos está especializado en la gestión de datos de salud y en la creación y revisión de publicaciones científicas. Nuestra máxima prioridad es trabajar para tu organización como si fuera la nuestra, de manera que saquemos el mayor partido a los datos y nos aseguremos de aplicar a cada estudio la metodología adecuada y el máximo rigor profesional. Sólo así conseguiremos recopilar eficazmente los datos y gestionarlos de manera cualificada para optimizar el desarrollo de tus ensayos clínicos y el flujo de datos.
Además, puedes tener plena confianza en que vamos a gestionar tus datos cumpliendo con la Buena Práctica Clínica, las normativas locales e internacionales (en especial la protección de datos: GDPR, HIPPA…), garantizando en todo momento la información del paciente y la confidencialidad.
Servicios de gestión de datos:
- Consultoría y diseño de protocolo
- Elaboración del Plan de Gestión de Datos (Data Management Plan, DMP) y todos los documentos asociados como el plan de consultas (Query Plan, QP), Case Report Form (CRF)…
- Servicios de entrada y revisión de datos
- Gestión de inconsistencias o queries, incluyendo comunicaciones y cierres
- Creación y validación de bases de datos, tanto en papel como en formato electrónico (eCRF) y ePRO
- Generación de conjuntos de datos (dataset) finales, de acuerdo con el CDISC (Clinical Data Interchange Standards Consortium), (Study Data Tabulation Model, SDTM; y Analysis Data Model, ADaM).
- Codificación médica.
- Reconciliación de AEs
- Transferencia de datos, integraciones e informes de datos personalizados.
Servicios de bioestadística:
- Planes de Análisis Estadístico (Statistical Analysis plans, SAP)
- Cálculo de muestras (N)
- Consultoría en estadística
- Aleatorización de pacientes, de acuerdo con los requisitos del protocolo.
- Creación del informe provisional de estudios clínicos y del informe del estudio clínico (Clinical Study Report, CSR).
Farmacovigilancia
Si buscas una solución de farmacovigilancia que conozca en profundidad los requisitos normativos tanto a nivel global como local, puedes contar con Sermes CRO. Nuestro equipo te garantiza obtener resultados a tiempo y en línea con el presupuesto acordado. Tenemos claro que llevar un correcto seguimiento de la seguridad de los medicamentos es una tarea compleja que sólo puede realizarse si están alineados los siguientes elementos: el proyecto, un exhaustivo control de calidad, la normativa y la fecha límite.
El equipo de expertos en farmacovigilancia de Sermes CRO se encargará de la interpretación, codificación y notificación de cualquier Acontecimiento Adverso o información relevante de seguridad.
Puedes contar con nosotros para:
- Preparación del Manual de Gestión de Seguridad
- Gestión de Acontecimientos Adversos Graves
- Código MedDRA
- Notificación de Reacciones Adversas Esperadas e Inesperadas en la base de datos de Eudravigilance
- Preparación y notificación del Informe Periódico de Seguridad (Periodic Safety Update Report, PSUR).
- Preparación de informes de seguridad

Medical Writing
Trabajamos en estrecha colaboración con nuestros clientes para poder preparar la de documentación de acuerdo con las necesidades y objetivos establecidos. Somos rápidos y flexibles, por eso entregamos documentos de alta calidad a tiempo. Nuestro equipo de profesionales cuenta con un gran conocimiento y experiencia en la preparación, elaboración y asesoría de toda aquella documentación relacionada con la investigación clínica. Además, nuestros clientes también confían en nuestra Unidad de Medical Writing para la revisión de documentos elaborados por ellos mismos y que necesitan de un empuje adicional en cuanto a asesoría científica y/o adaptación a las regulaciones vigentes.
Proporcionamos apoyo a nuestros clientes en la elaboración o revisión de:
- Diseño y creación de Protocolo, así como sus adaptaciones a la legislación vigente y BPC.
- Dossier del Producto en Investigación (IMPD) y/o Manual del Investigador (IB)
- Hoja de Información al Paciente y Consentimiento Informado, así como distintos materiales para los pacientes, como diarios, tarjeta del paciente, etc.
- Informe Clínico Final
- Dossier de Consulta Científica a Agencias Reguladoras (SA)
- Dossier de Designación de Medicamento Huérfano (ODD)
- Dossier de clasificación de medicamentos de terapias avanzadas
- Dossier para la Autorización de Liberación Voluntaria de OMG
- Informe Final de Liberación Voluntaria de OMG
- Dossier de Registro (CTD)
- Plan de Investigación Pediátrico (PIP)
- Publicaciones científicas: abstracts, posters, manuscritos, etc
Control de Calidad
- Preparación, apoyo e implementación de auditorías (documentación, hospitales, laboratorios…)
- Análisis y mejora de procesos
- Preparación y revisión de SOPs (Standard Operating Procedures)
- Evaluación de riesgos de auditorías y resultados de inspecciones, así como evaluación de implicaciones de la calidad general del proyecto
- Desarrollo de Acciones Correctivas y Preventivas (CAPA)
- Formación integral y eficaz
SERMES CRO es una empresa especializada en proporcionar servicios en investigación clínica a sus clientes: compañías farmacéuticas, empresas biotecnológicas e investigadores independientes. SERMES CRO proporciona apoyo en todo el proceso de desarrollo de nuevos medicamentos y terapias, desde las fases más tempranas hasta los estudios post-marketing. La prioridad de SERMES CRO es gestionar los ensayos clínicos con el objetivo de alcanzar los más altos estándares de Calidad, cumplimiento normativo, rentabilidad y plazos.
SERMES CRO está compuesta por un conjunto de profesionales técnicos cuya experiencia y formación garantizan el éxito en todos los servicios que presta a sus clientes logrando un amplio grado de fidelidad con los mismos.
Considerando el entorno cada vez más competitivo en el que desarrollamos nuestro trabajo, mantenemos nuestro compromiso profesional con todos nuestros clientes y el progreso médico y social, basándonos en una estructura de personal altamente cualificado con una gran flexibilidad y adaptación a sus necesidades; todo ello amparado bajo los estándares de la Calidad, y considerando en todo momento la importancia y cumplimiento de cualquier recomendación, código o normativa del sector, destacando las Buenas Prácticas Clínicas como principal factor de éxito para nuestra Empresa.
En SERMES CRO buscamos en todo momento la mejora continua en la prestación de nuestros servicios, así como en la atención y servicio al cliente. Con todo ello, garantizamos:
- El cumplimiento de los requisitos que nos aplican, así como de la normativa internacional y nacional que rige nuestro campo de actuación, tanto con el cliente/promotor como con todos los agentes que puedan intervenir en un ensayo clínico.
- Mantener la más alta capacitación y profesionalidad de nuestro personal en las actividades que realizan en el día a día, y gestionar el mejor uso de nuestros recursos humanos y materiales en pro de la satisfacción del cliente.
- La gestión de riesgos como pilar básico sobre el que trabajar, en aras de garantizar la mejor herramienta preventiva posible, y, con ello, la eficacia diaria empresarial que nos caracteriza.
- La total transparencia de nuestros objetivos de Calidad y rendimiento a la empresa, así como a nuestras partes interesadas.
El objetivo de SERMES, con todos los procesos establecidos, como la Política de Calidad, el resto de las herramientas del Sistema de Gestión de Calidad y la mejora continua, es conseguir y mantener la excelencia en el trabajo que realizamos.
La Dirección y la organización a todos los niveles de Sermes CRO demuestran su total compromiso con el Sistema de Gestión de Calidad mediante la comunicación y disposición de la presente Política de Calidad a todas las partes interesadas, según corresponda
Unidad de Contratos & Facturación
Optimizar el tiempo que dedicas a la gestión de contratos y la facturación de tus ensayos clínicos, ayudándote a mejorar tus procedimientos es el objetivo principal de nuestra Unidad de Contratos y Facturación. Llevamos más de una década alimentando nuestras herramientas de gestión con todo el conocimiento que hemos acumulado en la negociación de contratos, con el fin de ofrecer un servicio rápido y de calidad a nuestros clientes. Nos adaptamos a tus requisitos y te asesoramos sobre los diferentes tipos de clausulados legales.
¿Quieres que tus centros sean los primeros en incluir pacientes en tus ensayos, con un reclutamiento competitivo? El éxito está en los tiempos de negociación y firma de los contratos y en Sermes CRO somos especialistas en conseguir este hito.
Puedes contar con la experiencia de nuestro equipo especializado en contratos y facturación:
- Preparación de Financial Reports
- Diseño de estrategia de contratos
- Gestión de Acuerdos Jurídicos para regular un ensayo clínico, con hospitales, investigadores e instituciones colaboradoras.
- Asesoramiento legal en contratos de investigación clínica
- Gestión de documentación específica como acuerdos de confidencialidad, etc.
- Gestión de otro tipo de contratos como contratos de protección de datos, contratos de monitorización remota, etc.
- Calendarización de pagos, creación de órdenes de compra, solicitudes de facturas y pagos.
- Soluciones de pago de tasas, pago a hospitales e investigadores (en cualquier divisa).
Unidad de TMF & eTMF
Registrar, manipular y almacenar toda la información de los ensayos clínicos de manera que permita su interpretación y verificación de forma precisa es una labor diaria para el equipo de TMF de Sermes CRO. Contamos con más de 50 especialistas en TMF, que en la actualidad archivan documentos de ensayos clínicos desarrollados en más de 50 países.
Ya se trate de realizar labores de archivo en papel (TMF) o en formato digital (eTMF), en Sermes CRO contamos con las personas adecuadas para realizar este trabajo de manera excelente: a tiempo, con calidad y cumpliendo tanto con los procedimientos internos de nuestros clientes como con los requisitos normativos.
Nuestro equipo, altamente especializado y con gran experiencia en labores de TMF, garantiza la mayor calidad en la elaboración de TMFs, Archivo del Investigador (ISF) y Archivo de Farmacia (PSF).










